由军事科学院军事医学研究院陈薇院士领衔的科研团队自抵达武汉以来,就集中力量展开在疫苗研制方面的应急科研攻关,昨天(3月16日)20时18分,陈薇院士团队研制的重组新冠疫苗获批启动展开临床试验。

自1月26日抵达武汉以来,陈薇院士团队联合地方优势企业,在埃博拉疫苗成功研发的经验基础上,争分夺秒开展重组新型冠状病毒疫苗的药学、药效学、药理毒理等研究,快速完成了新冠疫苗设计、重组毒种构建和GMP条件下生产制备,以及第三方疫苗安全性、有效性评价和质量复核。昨天晚上,陈薇院士团队研制的新冠疫苗通过了临床研究注册审评,获批进入临床试验。中国工程院院士、军事科学院军事医学研究院研究员陈薇在接受总台央视记者独家采访时介绍,按照国际的规范,国内的法规,疫苗已经做了安全、有效、质量可控、可大规模生产的前期准备工作。
行行查,行业研究数据库 www.hanghangcha.com
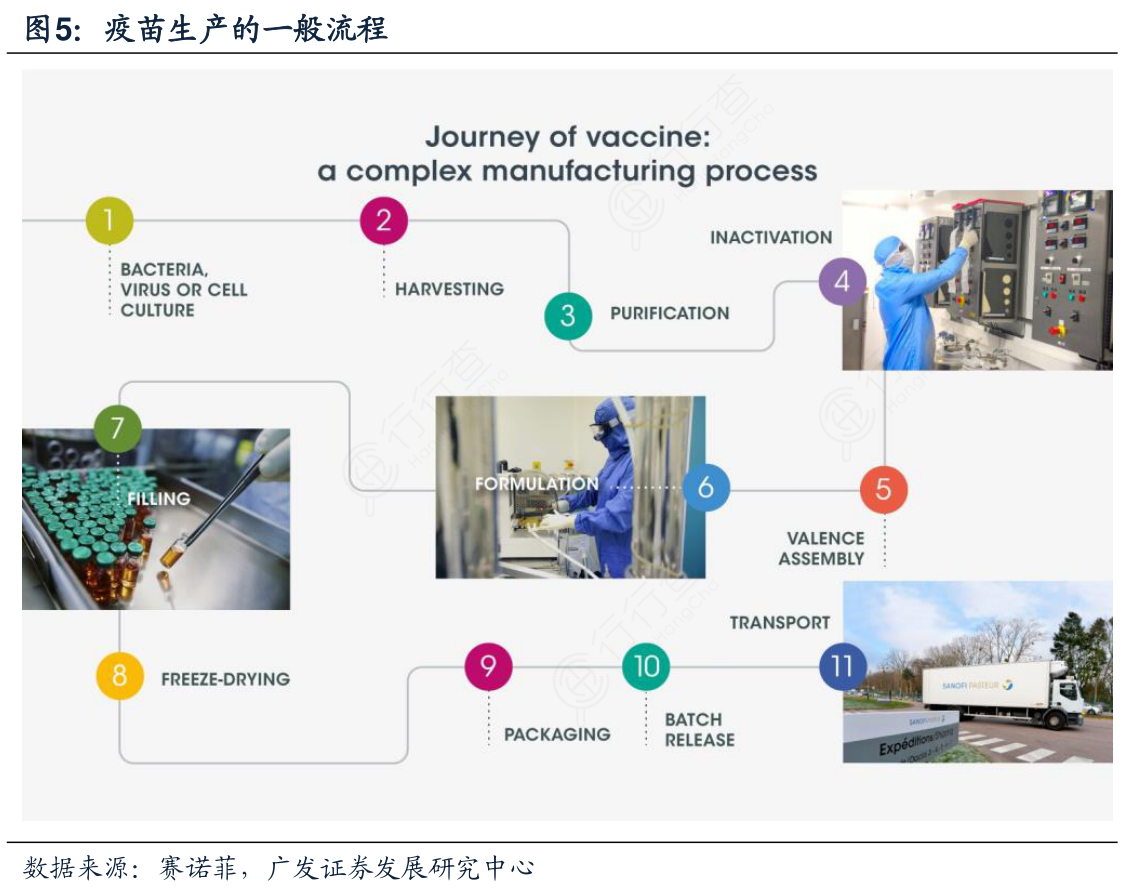
新型疫苗的研发周期通常需要10到15年的时间,临床研究、生产工艺与鉴定方法研究需协同一致。疫苗的总体开发通常包括临床研究、工艺开发以及鉴定方法的研究。


疫苗生产涵盖了制造疫苗的所有步骤:抗原生产、收获、纯化、灭活、配方(佐剂/防腐剂)、药物制备(灌装、检验和包装)的各个阶段以及质量控制,从生产流程上大致可以分为批生产与后处理,前者主要是生产出原液,后者是分装成制剂。疫苗的安全性、有效性通常与生产工艺的稳定性、鉴定方法以及质控体系密切相关。

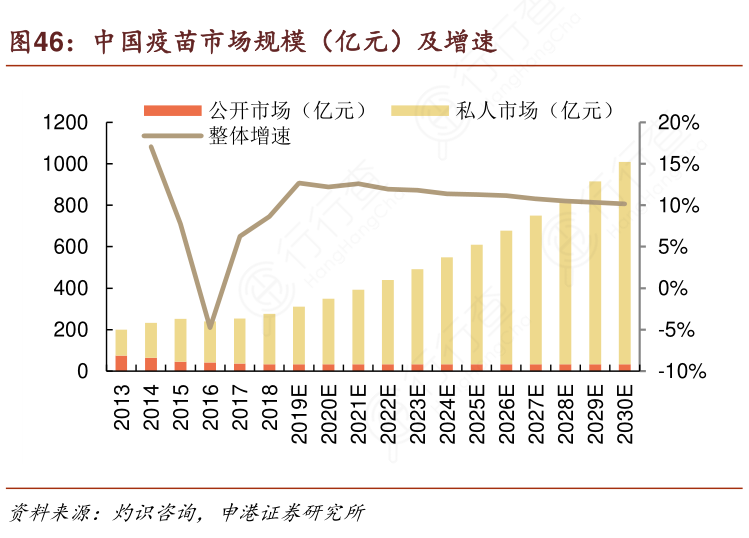
据灼识咨询数据,2018年我国疫苗整体市场规模达276亿元,增速8.7%,并预计随后12年CAGR可达11.4%,相对应全球疫苗预期12年CAGR仅6.4%,国内疫苗市场规模具备稳健预期。而短期疫情下对疫苗的重视程度进一步加强,或将进一步提振疫苗市场发展。

行行查,行业研究数据库 www.hanghangcha.com
手机访问“行行查”小程序更方便
![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()

![]()
