行业研究数据库
行业图谱研究
行业深度新闻

创业投资数据库
知名创投机构
重点项目动态

证券研究数据库
中国宏观数据
区域上市企业

2021-10-16
生命健康 | 行业数据
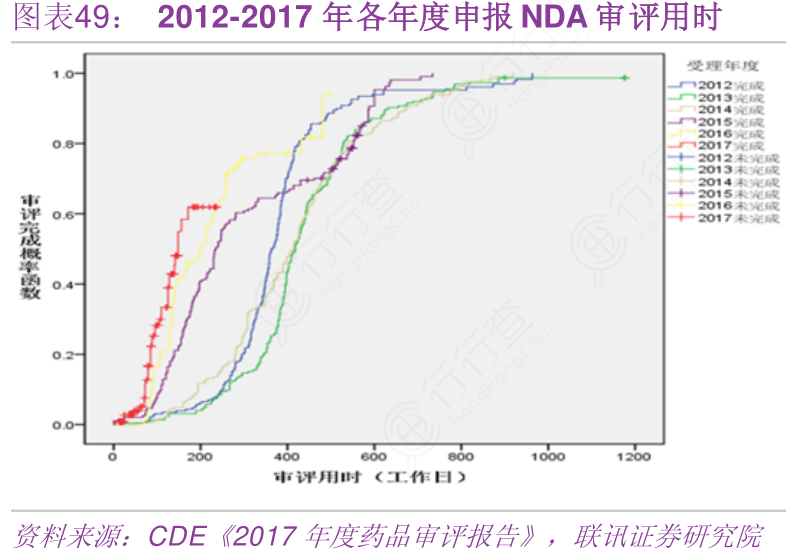
间。以化药为例,2017年,CDE共完成新药临床试验(IND)申请审评542件,IND申请首轮审评审批平均用时约为120个工作日,为法定时限(110个工作日)的1.09倍,基本实现按法定时限审评审批;CDE完成NDA申请审评236件,审评审批用时更是缩减明显。(备注:下图函数曲线越左移、越陡峭代表审评耗时越短,红色为2017年审评用时情况)
医药
登录网站查看更多数据
-
 咨询大家主营业务介绉确切的情况?
咨询大家主营业务介绉确切的情况?
-
 如何才能知道腾讯视频、爱奇艺、优酷土豆的运营策略对比的特点?
如何才能知道腾讯视频、爱奇艺、优酷土豆的运营策略对比的特点?
-
 各位网友请教下集工业属性与金融属性于一身的贵金属白银的真实信息?
各位网友请教下集工业属性与金融属性于一身的贵金属白银的真实信息?
- 04 想问下各位网友绝味食品在华南和华中门店数量多具体情况?
- 05 如何才能知道2015-2017磷酸铁锂和三元产能规划(GWh)(不完全统计)是怎样的呢?
- 06 想请教下各位H澳门GGR组成的真实信息?
- 07 你知道近三个月上市次新股盈利能力对比的情况?
- 08 谁知道2017年末,美国货币市场基金资金最终来的特点?
- 09 你知道山东开展危化品企业安全隐患排查整治紧急行动怎样的?
- 10 请问一下绝味食品以加盟模式为主,周黑鸭以直营模式为主实际的情况?




 行研数据库
行研数据库  图表数据
图表数据 
 研究报告
研究报告 
 产业数据
产业数据  创投数据库
创投数据库  创业投资
创业投资  基金备案
基金备案  城市经济
城市经济  证券数据库
证券数据库  招股书
招股书  证券研究
证券研究  上市发行
上市发行  商业数据库
商业数据库  专业数据
专业数据 








